Sportschool voor implantaat
Meike Kleuskens verdedigde op 23 september haar proefschrift bij de faculteit Biomedical Engineering.

Of het nu komt door een doodschop op het voetbalveld, of een ogenschijnlijk onschuldige botsing met de koffietafel: een kleine beschadiging aan het kraakbeen in je knie kan grote gevolgen hebben. In het ergste geval leidt de zwakke plek tot ernstige artrose en biedt alleen een kunstknie nog soelaas. Lapwerk in de vorm van een klein implantaat van opgekweekte kraakbeencellen zou erger kunnen voorkomen. Promovenda Meike Kleuskens ontwikkelde een ‘trainingsapparaat’ om te testen hoe dergelijke kraakbeenimplantaten zich gedragen als ze flink belast worden.
Je knieën krijgen nogal wat te verduren. Zelfs rustig wandelen stelt de knie al bloot aan continue druk-, rek- en schuifkrachten. Het flexibele kraakbeen in het kniegewricht heeft dan ook een ingenieuze structuur, vertelt Meike Kleuskens. “Door de bijzondere boogvorm van de elastische collageenvezels in het kraakbeen, worden krachten gelijkmatig over het weefsel verdeeld. We kunnen dat met de huidige implantaten nog niet nabootsen.”
Een relatief kleine beschadiging aan het kraakbeen tast die krachtverdeling al snel zodanig aan dat ook elders in het kniegewricht weefselschade ontstaat. Dat leidt tot kraakbeenslijtage en uiteindelijk zelfs aantasting van het omliggende bot. “Op een gegeven moment moet dan het hele gewricht vervangen worden door een kunstknie”, vertelt Kleuskens. “Dat is echter een zware ingreep, die je eigenlijk maar één keer wilt uitvoeren.” Helaas gaan kunstknieën slechts vijftien tot twintig jaar mee. Het is dan ook zaak de operatie zo lang mogelijk uit te stellen, zeker nu mensen steeds ouder worden.
Opkweken
Daarom wordt wereldwijd nu naarstig gezocht naar manieren om de opgelopen weefselschade direct te repareren, voordat het zijn verwoestende uitwerking kan hebben. Omdat er (nog) geen kunststof implantaatjes bestaan met de juiste eigenschappen, is de hoop gevestigd op tissue engineering, waarbij stukjes nieuw weefsel worden opgekweekt uit lichaamscellen - in dit geval kraakbeencellen -, ondersteund door een raamwerk (of ‘matrix’) van afbreekbaar kunststof. Dat opkweken kan zowel in het lab gebeuren als binnen het lichaam; na het implanteren vormt zich dan natuurlijk weefsel in het implantaat, terwijl de matrix geleidelijk wordt afgebroken.
Dat de knie zulke grote krachten aan moet kunnen, maakt de situatie extra ingewikkeld. Het blijkt dat een gebrekkige integratie van het implantaat in het omliggende weefsel er vaak toe leidt dat de ingreep niet de gewenste uitwerking heeft. Bovendien duurt het maanden voordat het implantaat als het ware ‘volgroeid’ is en die krachten ook daadwerkelijk aankan, legt Kleuskens uit. In haar promotieproject in de groep Orthopaedic Biomechanics van de faculteit Biomedical Engineering onderzocht ze daarom de omstandigheden waaronder dat opkweken van implantaten en integreren in bestaand kraakbeen het best verlopen. De basis voor haar onderzoek vormden cilindervormige ‘plugjes’ van kraakbeen op een schijfje bot van een centimeter in doorsnede.
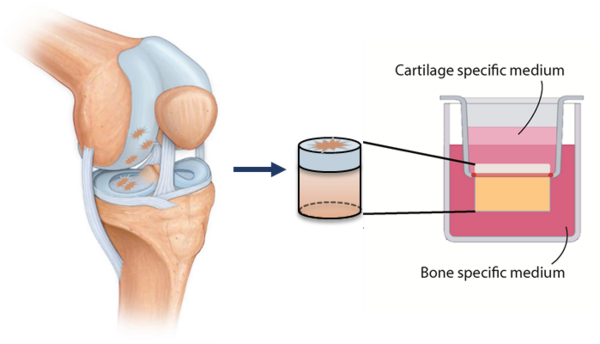
Kraakbeencellen doen helaas niet altijd wat je van ze verwacht. Cellen die je in een schaaltje opkweekt, zoals gebruikelijk, gaan vaak het verkeerde type collageen aanmaken, vertelt de Venlose. “Daardoor zijn die implantaten vaak niet succesvol, vooral niet in oudere patiënten.” In plaats daarvan zijn ze er bij Orthopaedic Biomechanics in geslaagd om driedimensionale stukjes weefsel te produceren in roerflessen met brokjes ondersteunend materiaal. Deze zogeheten organoïden, met een doorsnede van ongeveer 0,25 millimeter, implanteerde ze vervolgens in de kraakbeenplugjes.
De kraakbeencellen die Kleuskens gebruikte, waren afkomstig uit de verwijderde knieën van patiënten. Kraakbeen dus uit een aangetast gewricht van veelal oudere mensen. De vraag was of dat wel het juiste bronmateriaal is om vitaal kraakbeenweefsel uit op te kweken. “Ik heb de kweekresultaten daarom vergeleken met resultaten met kraakbeencellen van jongere, gezonde mensen afkomstig van het UMC Utrecht. Ik heb geen verschil gevonden met patiëntweefsel, dat dus prima geschikt lijkt om mee te werken. Dat is bovendien materiaal dat voldoende beschikbaar is en waarmee anders niets zou worden gedaan.”
Massage
Om een zo realistisch mogelijke situatie te creëren, bedacht ze ook een manier om de plugjes met verse implantaten bloot te stellen aan serieuze krachten. Samen met het uit de faculteit voortgekomen bedrijf LifeTec Group BV ontwikkelde de promovenda een soort trainingsapparaat, dat de plugjes aan een massage onderwerpt door middel van een stel zuigers met gladgepolijste koppen (zie de hoofdfoto). “Met dit apparaat bootsen we dus een lopend mens na.” Een maand lang, want zolang duurt het voordat kraakbeencellen in een nieuwe omgeving een collageenmatrix gaan vormen.
Het trainingsapparaat vormt - samen met de ontwikkelde kweektechnieken- volgens Kleuskens een goede methode om allerlei dingen in het lab uit te testen voordat er proefdieren in zicht komen. “Deze manier van werken kan de ontwikkeling van implantaten versnellen en het aantal proefdieren beperken.” En er is nog genoeg uit te zoeken in dit complexe onderzoeksveld. Zelf gaat ze liever op zoek naar een baan in het bedrijfsleven, maar ze hoopt dat er opvolgers voor haar worden gevonden bij Orthopaedic Biomechanics. “Ik heb een uitgebreide handleiding gemaakt, dus ik denk dat ook een student hiermee aan de slag zou moeten kunnen.”
Meer over gezondheid


Het laatste nieuws


