Nieuwe manieren om menselijke 'minibotten' te kweken
Bregje de Wildt onderzocht verschillende manieren om in het lab 'minibotten' te kweken, waarmee nieuw ontwikkelde geneesmiddelen voor botziekten kunnen worden getest.
Menselijke botten kunnen herstellen van kleine breuken, maar als de breuken te groot zijn of het hergroeiproces uit balans is, zoals het geval is bij osteoporose, is behandeling nodig. Om behandelingen te ontwikkelen worden vaak dierproeven gebruikt, maar sommige behandelingen die zo zijn ontwikkeld werken niet bij mensen. Daarom heeft Bregje de Wildt voor haar promotieonderzoek manieren onderzocht om menselijke 'minibotten' in het laboratorium te kweken die kunnen worden gebruikt om geneesmiddelen voor behandelingen te testen. Misschien maakt dit dierproeven voor het testen van dit soort geneesmiddelen in de toekomst overbodig.

Het menselijk lichaam vertrouwt op botten voor ondersteuning, voor bescherming van organen, voor beweging en voor opname en afbraak van mineralen. "Botten zien er misschien uit alsof ze star en statisch zijn, maar in werkelijkheid veranderen en evolueren botten altijd", zegt Bregje de Wildt, promovenda bij de faculteit Biomedical Engineering van de TU/e. "Cellen komen en gaan. Met name cellen die bekend staan als osteoclasten zorgen voor de afbraak en resorptie van bot, terwijl osteoblasten een even grote hoeveelheid nieuw bot vormen."
Het klinkt een beetje vreemd dat een botcel met 'blast' in de naam betrokken is bij de groei van bot, maar dit deel van de naam komt van het Griekse woord blastano, dat spruiten of ontkiemen betekent. "Samen dragen de osteoclasten en osteoblasten bij aan het vermogen van onze botten om te herstructureren of te regenereren. Kleine breuken zijn meestal een fluitje van een cent, maar voor grote breuken, of onevenwichtige activiteit van osteoclasten en osteoblasten bij aandoeningen als osteoporose, is behandeling nodig", vertelt De Wildt.
Ontwikkeling van de behandeling
Behandelingen voor botaandoeningen worden vaak ontwikkeld via dierproeven. Jaarlijks worden in Nederland ongeveer 500.000 dieren gebruikt voor proeven. Wereldwijd wordt dit aantal geschat op ongeveer 100 miljoen. "Helaas is minder dan 1 op de 10 behandelingen die met behulp van dierproeven zijn ontwikkeld ook effectief bij mensen, wat waarschijnlijk komt doordat de gebruikte dieren en mensen genetisch te verschillend zijn", aldus De Wildt.
Daarom besloten De Wildt en haar medewerkers van de onderzoeksgroepen Orthopedic Biomechanics en Bioengineering Bone dat het beste was om eerst menselijk botweefsel te gebruiken voor de evaluatie van de behandelingen voor menselijk botweefsel. "In plaats van een persoon te gebruiken om behandelingen te testen, wat op vele niveaus onethisch en riskant zou zijn, onderzochten we een manier om levende menselijke 'minibotten' te kweken in het laboratorium", zegt De Wildt.
Hoofdingrediënten voor tissue engineering
Om de ‘minibotten’ te kweken, had De Wildt vier belangrijke onderdelen nodig. Ten eerste had ze gespecialiseerde stamcellen nodig, de zogenaamde oudercellen. In tegenstelling tot pluripotente stamcellen, dat zijn cellen die elk type cel in het lichaam kunnen worden, kunnen de oudercellen alleen osteoblasten of osteoclasten worden. De Wildt: "Deze oudercellen moeten de juiste biochemische signalen ontvangen om te kunnen veranderen in osteoclasten en osteoblasten."
Ten tweede had de Wildt een structuur nodig waarop de botcellen konden samensmelten tot het 'minibotje'. "Hiervoor gebruikten we zijde van zijderupsen, omdat het een materiaal is met gunstige mechanische eigenschappen, het biocompatibel is, en menselijke cellen in drie dimensies op het materiaal kunnen groeien", zegt De Wildt.
Ten derde hebben de cellen een omgeving nodig waarin ze kunnen groeien en gedijen. "De cellen worden in een incubator geplaatst die op een temperatuur van 37 graden Celsius wordt gehouden, die daarnaast het zuurstof- en CO2-gehalte en de vochtigheidsgraad regelt", zegt De Wildt.
Om bot zoveel mogelijk na te bootsen, worden de botcellen tenslotte in een bioreactor geplaatst, die vervolgens in de incubator wordt geplaatst. De Wildt: "De bioreactor circuleert een voedingsvloeistof en bootst de mechanische belasting na van bot in het menselijk lichaam. Wil een 'minibot' representatief zijn voor echt bot, dan moeten de cellen worden uitgedaagd om deze krachten te weerstaan."
"Samen zijn dit de essentiële voorwaarden voor tissue engineering, dat sinds de jaren negentig in de regeneratieve geneeskunde wordt gebruikt om implantaten voor het lichaam te kweken," zegt De Wildt. "Recentelijk is tissue engineering echter gebruikt om in vitro versies van menselijk bot te maken, dat zijn versies van bot die buiten het menselijk lichaam zijn gekweekt."
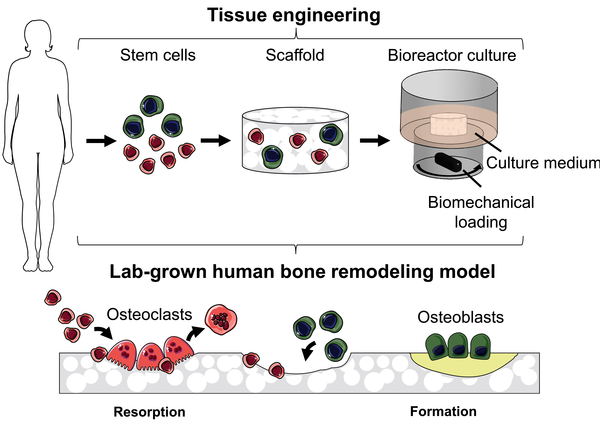
Verkenning van tissue engineering
Voor haar onderzoek onderzochten De Wildt en haar collega's een aantal verschillende aspecten van het in vitro kweken van de 'minibotjes'. In één onderzoek zochten ze naar een alternatief voor foetaal runderserum (afkomstig van een ongeboren koe) als voedingsbron voor de cellen. "We identificeerden een van mensen afkomstige vervanger voor het runderserum, die tot een nog betere groei van de 'minibotjes’ leidt", zegt De Wildt.
En in een ander onderzoek ontwikkelden De Wildt en haar collega's een methode om zijden steigers te mineraliseren. Mineralisatie in het menselijk lichaam is het proces waarbij zacht weefsel overgaat in hard weefsel. "We lieten ons inspireren door hoe bot zijn sterkte krijgt, wat samenhangt met hoe collageen en mineralen (zoals calcium en fosfaat) in het bot zijn georganiseerd. De gemineraliseerde zijden steigers ondersteunden de resorptie door osteoclasten en de vorming door osteoblasten. Deze miniatuurbenadering van het kweken van bot stelde ons in staat te bestuderen hoe bot wordt gestructureerd door menselijke cellen buiten het lichaam."
Behalve naar het voedingssupplement en het steigermateriaal keek De Wildt ook hoe veranderingen in de biochemische en biomechanische kweekomgeving invloed hadden op botresorptie en botvorming. "We varieerden de kweekomgeving om de in vivo omgeving in het menselijk lichaam beter te benaderen. Vervolgens bestudeerden we het effect van deze omgevingen op het evenwicht tussen botresorptie en -vorming, als kenmerk voor een gezonde hergroei van het bot", zegt De Wildt.
Hoop voor de toekomst
En De Wildt heeft grote verwachtingen van haar onderzoek, vooral gezien de prevalentie van botziekten. "Osteoporose is de meest voorkomende botziekte, die ongeveer 1 op de 5 mensen treft. Hoewel het niet dodelijk is, tast het de kwaliteit van leven aan en kunnen fracturen in bepaalde gevallen dodelijk zijn. Ik hoop dat dit onderzoek bijdraagt aan betere behandelingen voor botaandoeningen. Die zijn zeker nodig aangezien onze bevolking langer leeft en steeds meer mensen op latere leeftijd botproblemen krijgen."
Verder wil De Wildt graag dat haar onderzoek bijdraagt aan het veranderen van de manier waarop we in de toekomst behandelingen voor mensen testen. "Ik begrijp dat diermodellen nodig zijn om sommige onderzoeksvragen te beantwoorden. Maar ik heb moeite met het gemak waarmee ze voor onderzoeksdoeleinden worden gebruikt. In Nederland zijn de regels relatief streng, maar er zijn ook landen met beperkte regelgeving. Ik hoop dat mijn onderzoek zal bijdragen aan een verschuiving naar meer 'minibotten' ter vervanging van dierproeven in botonderzoek."
Titel van PhD-thesis: Advancing tissue engineering of in vitro human bone. Promotors: Sandra Hofmann en Keita Ito.
Mediacontact
Meer over gezondheid


Het laatste nieuws


