Weefselfysica speelt een sleutelrol in tumorgroei
Nieuw onderzoek toont aan hoe weefselfysica het RAS-gen helpt om vroege tumorontwikkeling aan te stimuleren.
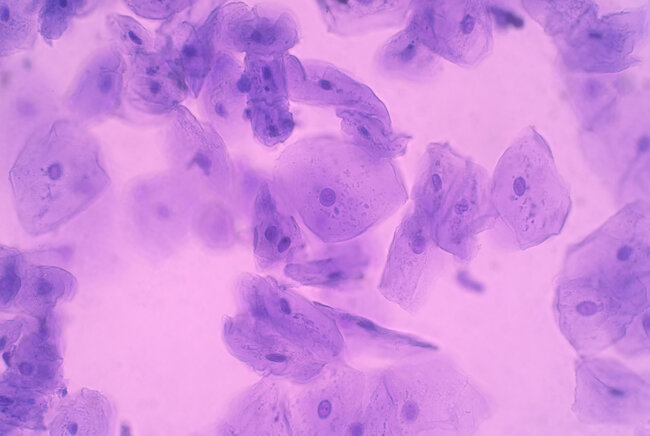
Kanker is moeilijk te behandelen en te bestuderen, en kan worden veroorzaakt door een reeks genetische mutaties. Zo veroorzaakt het gemuteerde RAS-gen een verlies van structuur in zogenaamd epitheelweefsel, een weefseltype dat de buitenkant van organen omhult. Om dit proces beter te begrijpen, hebben onderzoekers van de TU/e samen met collega's van IBEC in Spanje en UCL in het Verenigd Koninkrijk bestudeerd hoe het RAS-gen leidt tot tumorgroei in 2D-lagen van epitheelcellen. De resultaten wijzen erop dat weefselfysica een sleutelrol speelt bij tumorgroei, wat suggereert dat mechano-therapieën in toekomstige behandelingen zouden kunnen helpen bij de bestrijding van tumoren.
Kanker is een complexe familie van meer dan 200 verschillende ziekten, waarvan er veel meestal worden veroorzaakt door een gemuteerd gen, een oncogen. Een voorbeeld is het RAS oncogen, dat in ongeveer 30 procent van de gevallen van kanker bij de mens gemuteerd is, en dat structuurverlies veroorzaakt in epitheelweefsel, een type weefsel dat elk deel van het lichaam bedekt dat aan de buitenwereld wordt blootgesteld, en dat ook de buitenkant van organen bekleedt.
Het is zelfs zo dat epitheelweefsel de meest agressieve vormen van kanker voortbrengt: carcinomen. Recente gegevens suggereren dat weefselfysica een hoofdrol speelt bij het veranderen van de structuur van epitheelweefsel zodra het RAS-oncogen geactiveerd is.
Nieuw inzicht
Een nieuwe studie onder leiding van Vito Conte, van het Institute for Bioengineering of Catalonia (IBEC) en de TU/e, heeft een belangrijk inzicht verschaft in hoe de weefselfysica de expressie van het RAS oncogen regelt, en ook het daaruit voortvloeiende verlies van weefselstructuur tijdens de vroege stadia van tumorgroei.
"We weten al enige tijd dat kanker de fysica van weefsels verandert", zegt Conte. "We begrijpen nu langzamerhand dat de fysica van weefsels ook een rol speelt bij de progressie van kanker. Deze uitwisseling opent nieuwe wegen om de huidige therapieën te verbeteren, of zelfs nieuwe te creëren, zoals mechanosch-therapeutica."
Beginnen met een vel normale cellen
Om de structuur en functionaliteit van weefsel in stand te houden, werken epitheelcellen op een sterk gecoördineerde manier samen. De afbraak van de weefselstructuur is een sterke aanwijzing voor tumoren in epitheelweefsel, die tot 90 procent van alle kankers uitmaken.
Conte en zijn internationale team van onderzoekers wilden nagaan hoe de fysica bij dit proces betrokken is wanneer het RAS-oncogen in een enkele laag epitheelcellen wordt geactiveerd. "Het is moeilijk om mechanische veranderingen op cellulair niveau rechtstreeks in het menselijk lichaam vast te stellen. Onze grootste uitdaging was dus een manier te ontwikkelen om normaal menselijk weefsel in het lab te kweken, en vervolgens in real time de structuur en mechanica van tumoren in deze weefsels te volgen wanneer we het RAS-cogen aanzetten."
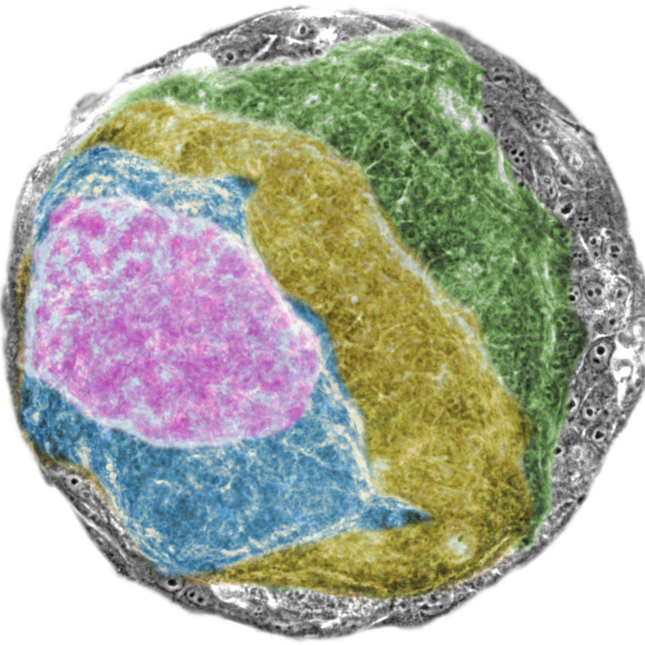
Van 2D naar 3D
De onderzoekers kweekten 2D-platen van epitheelcellen in het lab en activeerden het RAS-cogen in geselecteerde monsters. Binnen slechts 24 uur werden structurele en mechanische instabiliteiten waargenomen die het gevolg waren van een onevenwichtige verdeling van de intercellulaire krachten in de monsters.
In minder dan 48 uur was het door RAS geactiveerde weefsel getransformeerd in een 3D-massa, wat duidt op het begin van tumorgroei. Aan de andere kant, de niet-getransformeerde epithelia monsters behouden hun 2D controle structuur.
Nadere inspectie van de monsters met het geactiveerde RAS-oncogen toonde aan dat de cellen zich eerst in twee discrete lagen scheidden, waardoor het hele weefsel klaar was voor verlies van organisatie en de daaropvolgende vorming van een 3D-kankermassa. De onderzoekers ondersteunden hun experimentele bevindingen door de gegevens in een computersimulatie te modelleren.
Toekomstige mechano-therapieën
"Als we begrijpen waarom en hoe deze 2D naar 3D structuurverandering optreedt, is het mogelijk dat dit soort fysieke veranderingen in de toekomst gebruikt kunnen worden als indicatoren van carcinogenese, die dan aangepakt kunnen worden met mechano-therapieën", zegt Conte.
"Experimenteel bewijs dat de natuurlijke aard van kanker ondersteunt wordt steeds overweldigender en de scepsis uit het verleden is enigszins afgenomen", zegt Conte. "We moeten wel nog veel werk verzetten om de kankeronderzoeksgemeenschap (en de onderzoeksraden die ons onderzoek financieren) er volledig van te overtuigen dat er een meer inclusieve aanpak nodig is om kanker te bestuderen: een aanpak die mechanica combineert met biochemie, immunologie en moleculaire biologie."
'Oncogenic RAS instructs morphological transformation of human epithelia via differential tissue mechanics', Agata Nyga, José J. Muñoz, S.L. Dercksen, Giulia Fornabaio, Marina Uroz, Xavier Trepat, Buzz Baum, Helen K. Matthews, Vito Conte (2021).
Meer over gezondheid


Het laatste nieuws


